O mal de Parkinson é uma doença relativamente recorrente: uma estimativa realizada pelo noticiário R7 em 2018 levantou que 200 mil brasileiros vivem com a doença. Por isso, é de extrema importância saber quais são as pesquisas de cura e tratamento que estão sendo realizadas.
Quais Pesquisas Sobre a Doença de Parkinson Estão Sendo Realizadas?
O Instituto Nacional de Distúrbios Neurológicos e Derrame (National Institute of Neurological Disorders and Stroke) é o principal defensor da pesquisa biomédica no mundo. O NINDS conduz e apóia três tipos de pesquisas sobre a doença de Parkinson:
- Básica – descobertas científicas;
- Laboratorial/Clínica – desenvolvendo e estudando abordagens terapêuticas para a doença de Parkinson;
- Translacional – focado em ferramentas e recursos que aceleram o desenvolvimento da terapêutica na prática.
Estudos Clínicos
Os estudos clínicos sobre a doença oferecem uma oportunidade para ajudar os pesquisadores a encontrar maneiras melhores de detectar, tratar ou prevenir com segurança a doença de Parkinson.
Mas os estudos só podem ser concluídos se as pessoas se oferecerem para participar. Ao participar de um estudo clínico, indivíduos saudáveis e pessoas que vivem com a doença de Parkinson podem beneficiar grandemente a vida das pessoas afetadas por esse transtorno.
Modelos Animais
Os modelos animais são ferramentas valiosas para os cientistas que estudam os mecanismos da doença com o objetivo de desenvolver novos tratamentos para pessoas com Parkinson. Por exemplo, um estudo da droga isradipina – que havia sido demonstrado em animais para ter um efeito protetor sobre os neurônios dopaminérgicos – está sendo testado para um efeito neuroprotetor similar em humanos.
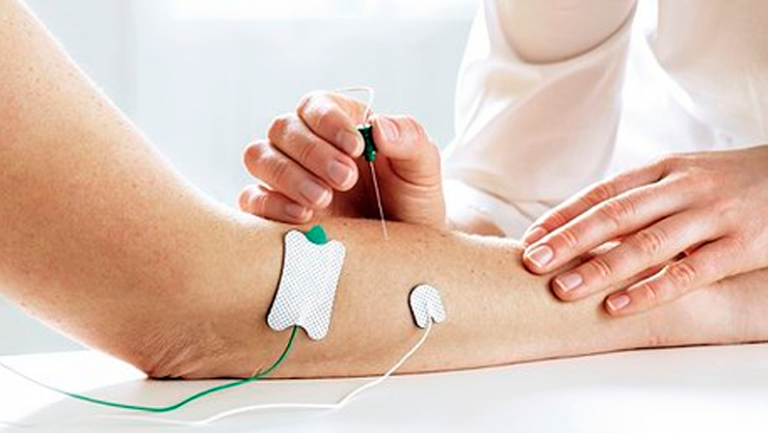
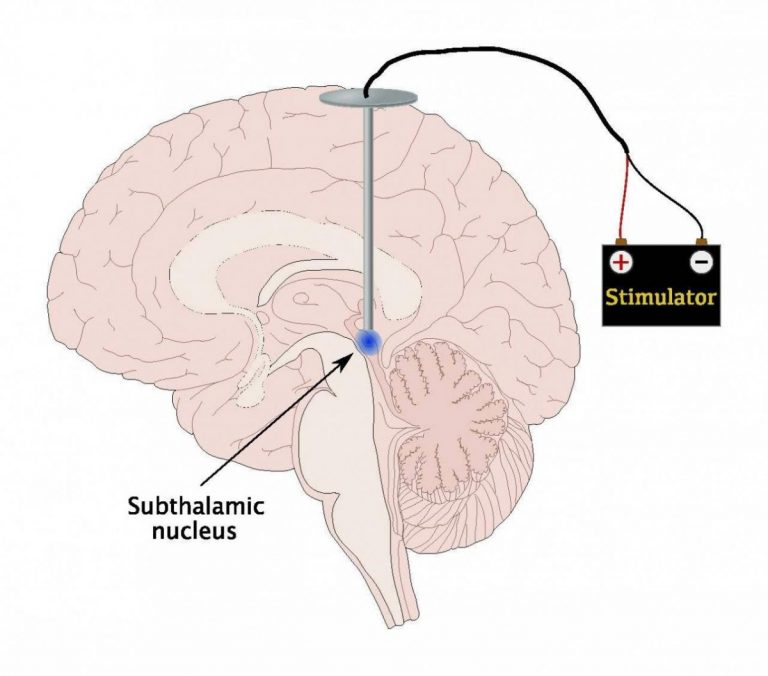
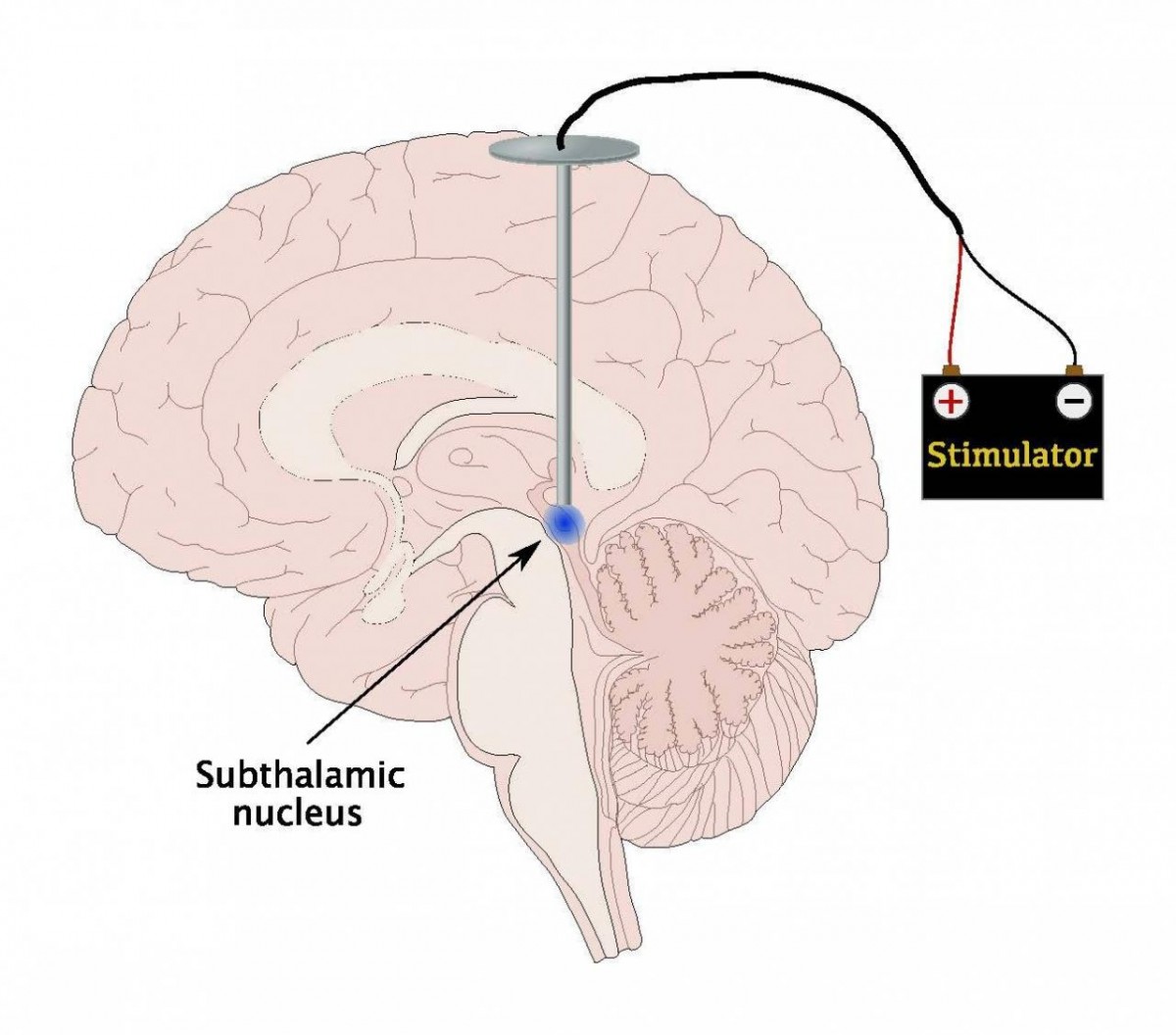
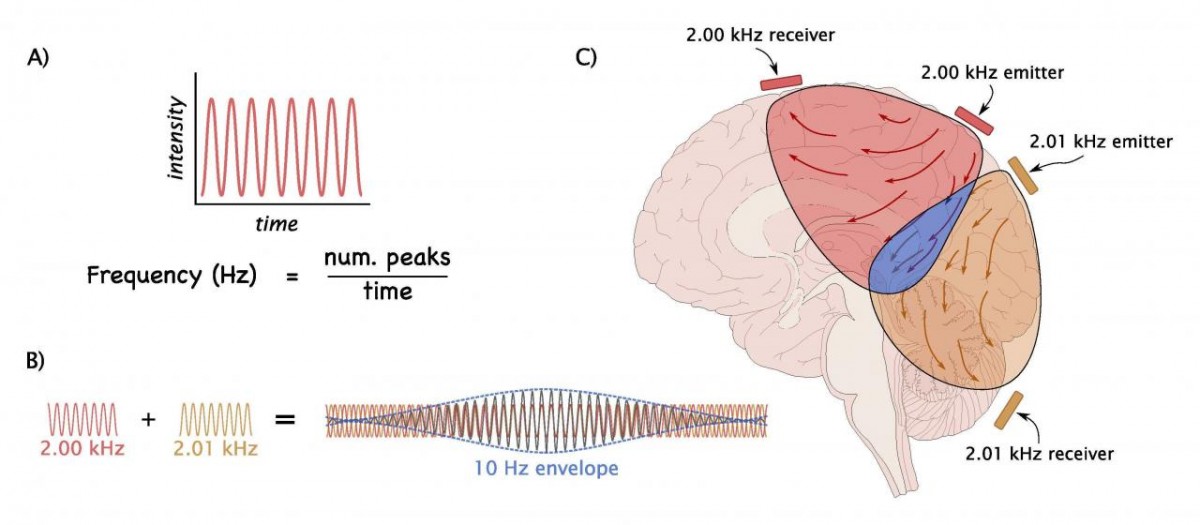
Estimulação Encefálica Profunda
Procedimento neurocirúrgico que envolve a aplicação de um dispositivo médico chamado neuroestimulador, que envia impulsos elétricos para alvos específicos no cérebro (núcleos cerebrais) por meio de eletrodos implantados. O procedimento é utilizado para o tratamento de distúrbios do movimento, incluindo doença de Parkinson. Além disso, é considerado uma opção de tratamento padrão para algumas pessoas que vivem com DP e cujos sintomas não respondem mais aos medicamentos para DP.
Exercícios Físicos
Os estudos sobre o mal de Parkinson também recomendam rotinas de exercícios para ajudar os indivíduos com DP a manter o movimento e o equilíbrio necessários para a vida cotidiana. Alongamento e tai chi são os mais recomendados.
Estudos Genéticos
Uma melhor compreensão dos fatores de risco genéticos está desempenhando um papel crítico na elucidação dos mecanismos da doença. Os estudos clínicos atuais incluem a conexão genética à memória e ao comportamento motor, a busca por genes que possam aumentar o risco de DP e distúrbios neurodegenerativos relacionados, e identificação de biomarcadores para DP.
Células-Tronco
Cientistas estão explorando vários tipos de células, incluindo células-tronco pluripotentes induzidas, como oportunidades para a descoberta de drogas para DP. A tecnologia dessas células-tronco será usada para definir os mecanismos da doença e descobrir os tratamentos mais promissores para a DP.
Busca de Soluções para os Sintomas de Complicações Motoras
Movimentos involuntários, incluindo discinesia (dificuldade de controlar o movimento muscular), tremores, distonia (contrações musculares involuntárias), incapacidade de caminhar e outras complicações motoras tornam-se evidentes à medida que a doença progride.
Estes sintomas costumam ser difíceis de tratar. Cientistas estudam a segurança e a eficácia de drogas e intervenções para aliviar os sintomas motores em pessoas com DP. Por exemplo, pesquisas utilizando a adenosina apontaram melhoras nas complicações motoras associadas à DP.
Outras pesquisas sobre a doença de Parkinson sendo realizadas incluem estudos sobre:
- Tratamentos dos sintomas de cognição e demência;
- Fatores de risco (exposição ocupacional repetida a certos pesticidas e solventes químicos, entre outros);
- Mitocôndrias (centenas de genes envolvidos na função mitocondrial são menos ativos em pessoas com DP);
- Fatores de crescimento do nervo;
- Drogas Neuroprotetoras.